GC-MS检测白酒中氨基甲酸乙酯方法的优化
GC-MS检测白酒中氨基甲酸乙酯方法的优化
刘 艳,周 玉1,刘 莎1,唐艳荣1,陆 瑶1,孙 莉2*
(1湖北信嘉检测科技有限公司,湖北咸宁 437100;2.黄鹤楼酒业有限公司,湖北武汉 430050)
作者简介:刘艳(1984—),女,湖北咸宁人,专科,助理工程师。研究方向:酒类安全与检测。
通信作者:孙莉(1983—),女,湖北武汉人,本科,助理工程师。研究方向:酒类安全与检测。E-mail:h-sunli1@gujing.com.cn。
摘 要:本文根据《
金博宝188官网注册 国家标准 食品中氨基甲酸乙酯的测定》(GB 5009.223—2014)对白酒中的氨基甲酸乙酯进行检测,过程中对GC-MS检测方法进行了优化,该方法高效准确且稳定性好,回收率为99.6%~103%,相对标准偏差为0.5%~4.4%,能够满足白酒中氨基甲酸乙酯的测定要求。
关键词:氨基甲酸乙酯;GC-MS;白酒
氨基甲酸乙酯(Ethyl carbamate,简称EC,分子式为H2NCOOC2H5),又称尿烷,是食物在发酵或者存储过程中天然产生的物质。氨基甲酸乙酯是一种可以引起肺肿瘤、淋巴癌、肝癌、皮肤癌等疾病的可致癌物质。发酵食品中含有氨基甲酸乙酯是
金博宝188官网注册 的潜在危害[1],因此,对食品中氨基甲酸乙酯含量的检测是对消费者健康安全的保障。氨基甲酸乙酯是一种具有潜在致癌作用的化合物,存在于传统的发酵食品中;乙醇对氨基甲酸乙酯的致癌性有促进作用[2],国际癌症研究署在1987年将其归为2B类致癌物质,在2007年对其进行再次评估后改为2A类致癌物。加拿大卫生与防疫部门规定蒸馏酒中氨基甲酸乙酯的限量为150 µg/L,我国目前未对氨基甲酸乙酯出台相关的限量标准。目前,酒中的氨基甲酸乙酯的检测方法有高效液相色谱法、气相色谱法。其中液相色谱法前处理操作复杂且效率不高;而气相色谱-质谱法有着对样品的前处理损耗低、灵敏度高、分析效率高等特点,在对氨基甲酸乙酯检测的应用中最为广泛。本文对《金博宝188官网注册 国家标准 食品中氨基甲酸乙酯的测定》
(GB 5009.223—2014)的方法进行了一定的改进,更换了GC-MS的色谱柱[3],以及洗脱液[4-5],选择了稳定的萃取方法[6],能够安全有效地对白酒中的氨基甲酸乙酯进行检测。
1 材料与方法
1.1 试剂及仪器
试剂:氯化钠(NaCl);正己烷(C6H14)色谱纯;甲醇
(CH40)色谱纯;二氯甲烷(CH2Cl2)色谱纯;氨基甲酸乙酯专用萃取柱(CLEANERT)。
标准品:氨基甲酸乙酯标准品(C3H7O2N;CAS:51-79-6)纯度>99.0%;D5-氨基甲酸乙酯标准品(C3H2D5NO2;CAS:73962-07-9)纯度>99%。
样品:市售白酒、自酿原酒。
仪器:气相色谱-质谱联用仪(安捷伦8860-5977B);全自动固相萃取仪(睿科FS360);氮吹仪;电子天平;漩涡振荡混合器;超声波清洗机。
1.2 试验方法
1.2.1 标准溶液配制
(1)D5-氨基甲酸乙酯储备液(1.00 mg/mL)。准确称取0.01 g(精确到0.000 1 g)D5-氨基甲酸乙酯标准品,用甲醇溶解,定容到10 mL,备用。
(2)D5-氨基甲酸乙酯使用液(2.00 µg/mL)。取D5-氨基甲酸乙酯储备液(1.00 mg/mL)0.10 mL,用甲醇定容至50 mL,备用。
(3)标准储备液(1.00 mg/mL)。称取0.05 g(精确到
0.000 1 g)氨基甲酸乙酯标准品,用甲醇溶解并定容至50 mL。
(4)标准中间液①(10.0 µg/mL)。取氨基甲酸乙酯储备液(1.00 mg/mL)1.00 mL,用甲醇定容至100 mL,备用。
(5)标准中间液②(0.50 µg/mL)。取氨基甲酸乙酯中间液①(10.0 µg/mL)5.00 mL,用甲醇定容至100 mL,备用。
(6)标准曲线的配制。分别吸取标准中间液②(0.50 µg/mL)20.0 µL、50.0 µL、100.0 µL、200.0 µL、400.0 µL和标准中间液①(10.0µg/mL)40.0 µL、100.0 µL于7个1 mL容量瓶中;各加入D5-氨基甲酸乙酯使用液(2.00 µg/mL)100 µL,甲醇定容。使D5-氨基甲酸乙酯浓度为200 ng/mL,标准曲线浓度分别为10.0 ng/mL、25.0 ng/mL、50.0 ng/mL、100.0 ng/mL、200.0 ng/mL、400.0 ng/mL和1 000.0 ng/mL。
1.2.2 样品前处理
准确量取2.00 mL酒样于10 mL玻璃试管中,称重并记录酒样的质量m(精确到0.001 g);加入100.0 µLD5-氨基甲酸乙酯使用液(2.00 µg/mL),再加入0.3 g氯化钠(经过640 ℃烘2 h),超声溶解,再转移到萃取柱中。固相萃取仪设置的样品制备流程见表1
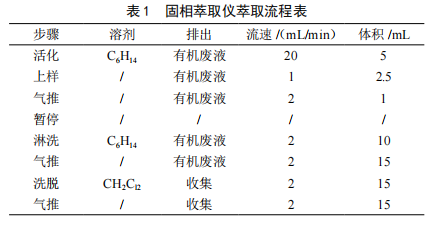
将洗脱液在室温下用氮气缓缓吹至约0.5 mL,用甲醇定容到1.00 mL,此为待测液,供GC-MS检测分析。
1.2.3 仪器条件
色谱柱:DB-WAX UI柱(60 m×0.25 mm×0.25 µm);进样口温度220 ℃;柱温:初始温度50 ℃,以15 ℃/min速率升至155 ℃,再以5 ℃/min的速率升至185 ℃后运行:240 ℃运行5 min。不分流进样;进样体积1 µL;载气:氮气(纯度≥99.999%);流速1 mL/min;电离模式:EI源,离子源温度230 ℃;四极杆温度150 ℃;溶剂延迟11 min。氨基甲酸乙酯选择监测离子(m/z):44、62、74、89;定量离子:62;D5-氨基甲酸乙酯选择监测离子(m/z):64、76;定量离子:64。
2 结果与分析
2.1 内标物的选择
该方法的内标物为D5-氨基甲酸乙酯,其是与氨基甲酸乙酯具有相同分子结构的稳定同位素,且具有一致的物理化学性质,能够有效消除基质效应和前处理等因素对分析结果的影响;在色谱分析中又能与待测物进行充分地分离;最重要的是D5-氨基甲酸乙酯是一种人工合成物质,无法在生产过程中自然产生。这些特点使D5-氨基甲酸乙酯作为该检测方法的内标物,大大优于氨基甲酸丙酯。
此分析方法在预处理前加入内标物,当混合溶液中的待测物和内标物的比值恒定时,可以消除在预处理过程中带入的不稳定性因素的影响。
2.2 洗脱溶液的选择
此方法的洗脱液使用的是二氯甲烷。二氯甲烷无色透明,易挥发,具有类似醚的轻微刺激味道,且毒性小,稳定性高,可很好地吸附固相萃取柱中的氨基甲酸乙酯;又因其易挥发,氮吹时能大大节约时间,提高效率;《金博宝188官网注册 国家标准 食品中氨基甲酸乙酯的测定》(GB 5009.223—2014)中所使用的5%乙酸乙酯-乙醚溶液,具有强烈的刺激性气味,在通风良好的环境也会对操作者的眼睛及呼吸系统也会产生强烈刺激,不利于操作者的身心健康。因此,该方法选择了二氯甲烷作为洗脱液,二氯甲烷在通风良好的空间中气味小,有更好的环保安全性。
2.3 色谱柱的选择
本试验选择的是DB-WAX UI柱(60 m×0.25 mm×
0.25 µm)。该色谱柱为超惰性色谱柱,不易与化合物产生吸附作用,固定相可用溶剂冲洗,并可耐受水溶液进样。在分析时能够更加有效地分离氨基甲酸乙酯,提供对称的峰形和更高的响应。且该色谱柱可以检测部分农药残留的检测项目,适用范围广泛,适用性强。氨基甲酸乙酯与其内标物的峰形完整且完全分开。该方法的内标物在12.19 min出峰,目标物在12.27 min出峰。
2.4 工作曲线及线性
取1.2.1中所配制的标准曲线的样品,用设定好的仪器条件对其进行检测。以浓度(ng/mL)为X轴,响应(峰面积)为Y轴,绘制的标准曲线为Y=98.566X-542.66,R2=0.999 7。氨基甲酸乙酯标准曲线及线性图见图1。
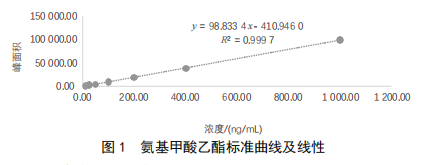
2.5 准确度和精密度
用本方法对市售白酒和自酿原酒进行分析,根据样品的氨基甲酸乙酯含量和曲线浓度范围,添加了不同浓度的加标样进行检测。样品的回收率为99.6%~103%;相对标准偏差为0.5%~4.4%。样品回收率测定结果及精密度试验结果分别见表2和表3。
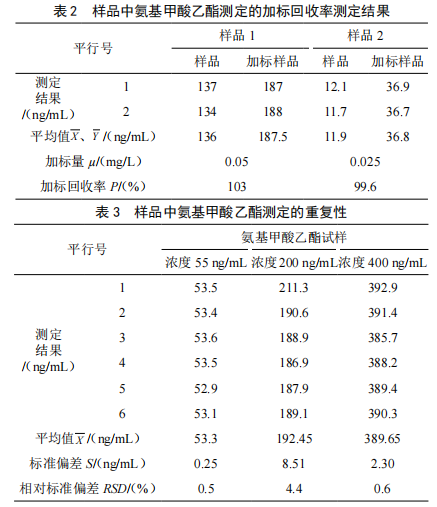
3 结论
本文讨论了GC-MS检测白酒中的氨基甲酸乙酯的新方法,着重讨论了样品前处理的洗脱液,色谱柱的使用以及对内标物的选择,并分析了其优缺点。同时通过试验得出该方法检测的回收率为95%~105%;相对偏差为0.5%~4.5%。经过优化后,对氨基甲酸乙酯的检测具有良好的灵敏度、准确度和精密度,能够满足白酒中氨基甲酸乙酯的测定要求。
与《金博宝188官网注册 国家标准 食品中氨基甲酸乙酯的测定》(GB 5009.223—2014)相比较,本方法选择了D5-氨基甲酸乙酯作为内标物,避免了样品的基底效应;更换了洗脱溶液,避免了乙酸乙酯的刺鼻气味,使得前处理简单高效;更换了色谱柱,提高了灵敏度的同时也提高了色谱柱的应用的广泛性。
参考文献
[1]丁霞.酒醅中氨基甲酸乙酯及其前体的控制与消除[D].无锡:江南大学,2018.
[2]卓俊纳,吴卫宇,陈静,等.三种香型白酒中氨基甲酸乙酯的研究及聚类分析[J].酿酒科技,2021(8):22-27.
[3]刘楚楚,陈二芳,刘倩倩.基于GC-MS测定白酒中氨基甲酸乙酯的探讨[J].酿酒,2021,48(1):120-123.
[4]周韵,寸宇智,李长寿,等.GC-MS法测定白酒中氨基甲酸乙酯[J].云南化工,2018,45(8):68-70.
[5]梁孟军,张瑞雨,荣国琼,等.不同酒类中氨基甲酸乙酯前处理方法的研究[J].职业与健康,2014,30(16):2320-2322.
[6]郭学武,李园子,黄世永,等.GC-MS测定白酒中氨基甲酸乙酯的不同预处理方法的比较[J].现代食品科技,2016,32(4):249-253.

相关热词搜索:
[责任编辑:]



 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
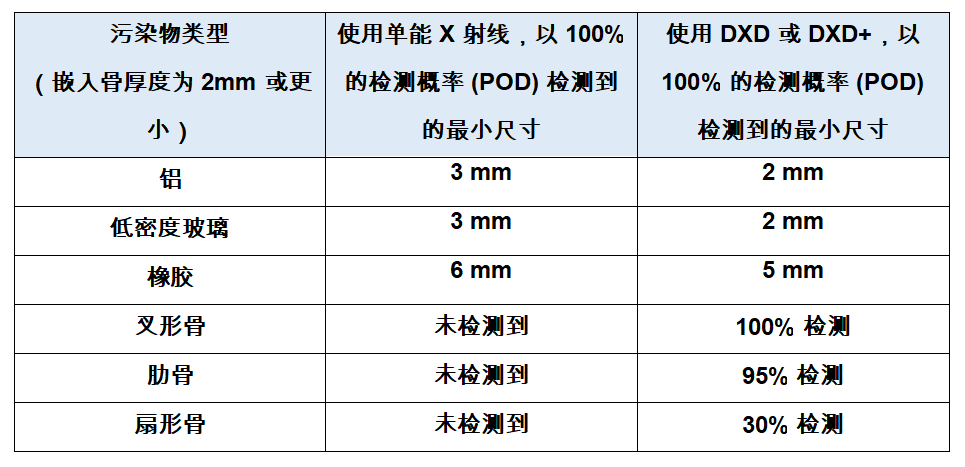 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《金博宝188官网注册 最佳实践白皮书(2021-2022年)》四大主题发布
《金博宝188官网注册 最佳实践白皮书(2021-2022年)》四大主题发布

 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨  凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高  精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在  《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布! 





参与评论