西青果颗粒在多种溶出条件下溶出曲线测定及溶出机制研究
宋韶锦,巩腾飞*,孟庆山,张 羽
(威海市食品药品检验检测研究院,山东威海 264200)
摘 要:目的:测定西青果颗粒在不同溶出条件下溶出曲线并分析其溶出机制。方法:采用HPLC法检测没食子酸含量,浆法、小杯法作为溶出测定方法,测定西青果颗粒在不同溶出介质(蒸馏水、0.1 mol/L盐酸溶液)、搅拌速度
(50 r/min、75 r/min、100 r/min)的溶出曲线,Origin软件分析西青果颗粒的溶出机制。结果:HPLC法测定西青果颗粒溶出方法准确稳定;浆法测定西青果颗粒在不同溶出条件下溶出曲线相似,在10 min累计溶出率均高于80%;小杯法测定西青果颗粒溶出曲线对一级动力学拟合相关性系数均高于0.99。结论:西青果颗粒溶出迅速,满足颗粒剂的制剂要求,溶出机制为Fick扩散。
关键词:西青果颗粒;没食子酸;溶出曲线;溶出机制
西青果又称“藏青果”,为使君子科植物诃子( Retz.)的干燥幼果,在中医临床中作为清热解毒药用于复方配伍治疗肺炎、喉炎、扁桃体炎、咽炎、细菌性痢疾等症[1]。西青果中鞣质与酚酸类成分含量丰富,主要化学成分为诃子酸、诃黎勒酸及没食子酸等[2-3]。西青果颗粒是由西青果水提醇沉物经制剂化制备的中成药颗粒,在临床用于治疗咽喉干痛、慢性扁桃体炎等疾病[4]。进行中药颗粒制剂的体外溶出度评价研究是有效的制剂质量控制手段,有利于指导制剂的处方优化与制剂质量标准的建立[5]。本文旨在比较不同溶出度测试方法对西青果颗粒溶出行为评价的影响差异,考察西青果颗粒在不同溶出条件下的溶出行为适应性及进行溶出机制分析。
1 材料与方法
1.1 仪器与试剂
岛津LC-20AT高效液相色谱仪(日本岛津公司);Hypersil C18色谱柱(250 mm×4.6 mm,5μm);MS105DU电子天平(梅特勒-托利多仪器(上海)有限公司);RCZ-8B溶出试验仪(天津市天大天发科技有限公司);UV-2550紫外可见分光光度计(日本岛津公司)。
甲醇(色谱纯,默克);磷酸(天津市科密欧化学试剂有限公司);水为自制重蒸水;其他试剂未经说明均为分析纯。没食子酸标准品(中国药品食品检定研究所,批号110831-201605,含量90.8%);西青果颗粒(广西天天乐药业股份有限公司,15 g×10袋)。
1.2 没食子酸含量分析方法建立
1.2.1 色谱条件
Hypersil C18色谱柱(250 mm×4.6 mm,5 μm);SPD-10A
型二极管阵列检测器;柱温25 ℃;流动相为以甲醇-0.5%磷酸水溶液(15∶85);流速0.8 mL/min;检测波长215 nm,进样量20 μL。
1.2.2 供试品溶液制备
取样品10袋,研细,精密称定一定量的细粉约0.3 g,
平行两份于具塞锥形瓶中,分别以50%甲醇、水和0.1 mol/L
盐酸为溶剂,精密加入溶剂25 mL后称定重量,超声处理20 min(功率250 W,频率40 kHz),超声的过程中要不断的变换瓶子的相对位置,以便于超声均匀,再用对应的溶剂补足失重后,摇匀,用0.45 μm的滤膜过滤,采用HPLC法测定。
1.2.3 对照品溶液制备
精密称定没食子酸对照品11.36 mg,置于100 mL容量瓶,50%甲醇溶液溶解定容,微孔滤膜(0.45 μm)过滤,制备得浓度为103.15 μg/mL没食子酸对照品原始液,备用。
1.2.4 标准曲线制备
50%甲醇溶液对浓度为103.15 μg/mL没食子酸对照品原始液进行梯度稀释,得到浓度为1.031 5 μg/mL、10.315 μg/mL、20.63 μg/mL、41.26 μg/mL、61.89 μg/mL、82.52 μg/mL和103.15 μg/mL的系列浓度溶液。HPLC进样
20 μL测定后以峰面积(Y)对浓度(x)拟合回归方程。
1.2.5 精密度考察
移取没食子酸对照品原始液,重复进样6次,记录峰面积。
1.2.6 稳定性考察
移取新配制的没食子酸对照品溶液,于0 h、4 h、8 h、12 h、16 h、24 h和48 h时间点分别进样测定。
1.2.7 重复性考察
分别以50%甲醇溶液、蒸馏水、0.1 mol/L盐酸溶液为溶剂溶解定容没食子酸对照品,所得样品溶液分别于0 h、4 h、8 h、12 h、16 h、24 h和48 h时间点分别进样测定。
1.2.8 加样回收率考察
分别精密量取1.2.2项3种溶剂的样品溶液1 mL,置于50 mL容量瓶中,分别加入1.2.3项下没食子酸对照品溶液1 mL,再分别用相对应的溶剂稀释定容至刻线,0.45 μm的滤膜过滤,HPLC法测定。
1.3 溶出度测定
1.3.1 浆法
西青果颗粒1袋,采用2015年版《中国药典》附录溶出度测定第二法浆法,溶出介质体积为800 mL,于不同设置转速下在(37±0.5)℃下进行西青果颗粒剂的溶出测定。在设置取样时间点(10 min、20 min、30 min、40 min、50 min、60 min、70 min、80 min、90 min、100 min、110 min和120 min)利用自动取样系统取样5 mL,并及时补充等温等量溶出介质。为保证取样准确性与自动取样系统的运行稳定性,取样针配制0.45 μm滤头以防止取样未溶解细小
颗粒。
1.3.2 小杯法
基于小杯法测定西青果颗粒溶出的测试方法除溶出介质体积设置为200 mL利用自动取样系统取样1 mL,并及时补充等温等量溶出介质,向取样管中精密加4 mL的溶出介质混匀制成样品,其他参数与1.3.1项下浆法参数一致。
1.4 西青果颗粒在不同测试条件下溶出曲线绘制
西青果颗粒1袋,参照1.3.1项下浆法与1.3.2项下小杯法溶出度测定方法,在不同溶出介质(蒸馏水、0.1 mol/L盐酸溶液)和搅拌速度(50 r/min、75 r/min、100 r/min)组合条件下进行西青果颗粒的溶出测试,溶出样品经HPLC进行含量测定,绘制溶出曲线。
1.5 西青果颗粒溶出机制分析
利用Origin数据分析软件对西青果颗粒小杯法测定溶出曲线分别进行零级动力学、一级动力学、Higuchi方程以及Korsmeyer- peppas方程动力学方程拟合,寻找最佳描述和预测西青果颗粒溶出行为的数学模型。
2 结果与分析
2.1 没食子酸含量分析方法建立
没食子酸回归方程为=105 934-1 465.3,相关系数2=0.999 9,结果表明没食子酸在1.0315~103.15 μg/mL范围内线性关系良好。精密度考察峰面积的为0.45%(=6),表明方法精密度良好。稳定性考察没食子酸峰面积的为1.49%(=7),表明没食子酸对照品溶液在
48 h内稳定。
重复性考察(=7)和加样回收率(=3)的结果见表1,通过数据可以表明,没食子酸在不同溶液之间的重复性良好,且加样回收率符合定量测定要求。
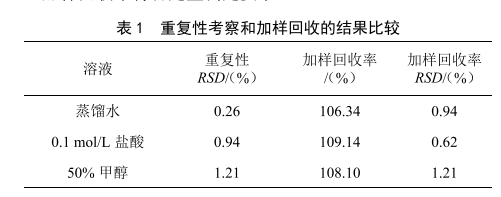
2.2 不同溶剂的含量结果比对
通过数据比较可以得出,不同溶剂之间含量测定的比对结果显示,蒸馏水、50%甲醇溶液、0.1 mol/L盐酸溶液的含量测定结果偏差较小。实验数据结果见表2。
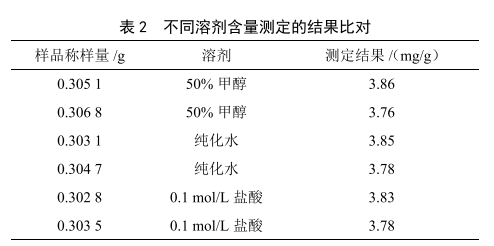
2.3 西青果颗粒在不同测试条件下溶出曲线绘制
由表3、表4可知,西青果颗粒浆法测定,在不同溶出介质、不同搅拌速度的组合测试条件下,在10 min的累计溶出率均高于80%,溶出迅速,符合颗粒剂快速溶出的制剂要求。以浆法作为测试方法,以蒸馏水作为溶出介质时,西青果颗粒在搅拌速度分别为50 r/min、75 r/min、100 r/min条件下,10 min时的累计溶出率分别为84.44%、91.63%、91.06%,溶出达平台期时间分别为20 min、10 min、10 min,说明搅拌速度可影响溶出药物的扩散速率从而影响制剂溶出。溶出曲线测定时搅拌速度的设定应模拟体内生理环境。为了在体外制剂研究时更好控制制剂质量,确保制剂在多种体内环境均有较好溶出适应性,应考察制剂在低搅拌速度(50 r/min)下的溶出曲线,以预测制剂在患者体虚状态胃肠蠕动功能低下时的溶出性能。西青果颗粒在50 r/min搅拌条件下在蒸馏水和0.1 mol/L盐酸溶液两种溶出介质中均可快速溶出,颗粒在不同搅拌速度下的溶出适应性较好。浆法测定西青果颗粒溶出时,在不同搅拌条件下,颗粒剂在蒸馏水和0.1 mol/L盐酸溶液中的溶出曲线较为相似,颗粒剂在不同溶出介质中的溶出适应性较好。

小杯法与浆法相比,是在更小体积的溶出介质中进行的固体制剂溶出测试。以小杯法作为测试方法测定西青果颗粒的溶出曲线,在相同溶出介质中,搅拌速度影响西青果颗粒剂的溶出,这与浆法测定结果一致。当溶出介质相同,所选择的转速不同时,其相同时间段内表现出来的累计溶出率之间存在着一定的差异,具体数据可以参见表2。以上结果说明西青果颗粒在小杯法中的溶出慢于浆法测定,其原因可能为由于溶出介质体积差异导致的剪切速率与没食子酸扩散速率的差异。
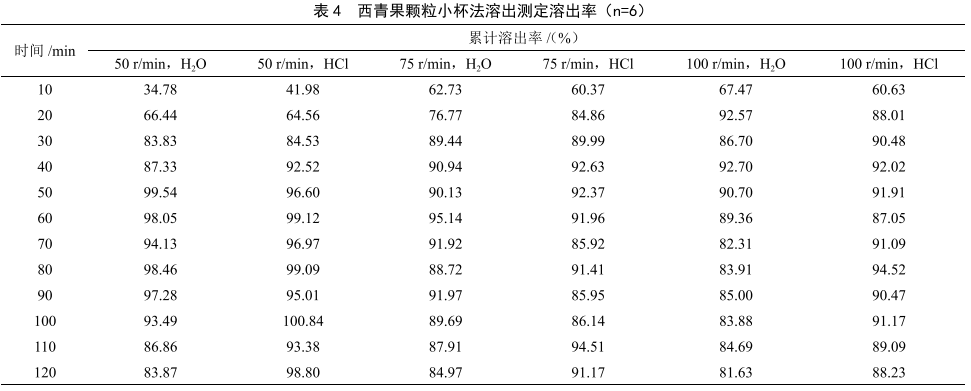
2.4 西青果颗粒溶出机制分析
拟合结果表明,西青果颗粒在各种溶出条件下小杯法测定溶出曲线对一级动力学的拟合相关性系数均高于0.99。在低搅拌速度(50 r/min)对一级动力学方程与Higuchi方程拟合较好,拟合相关系数均高于0.99,表明西青果颗粒的溶出机制为Fick扩散,颗粒溶蚀对其溶出存在一定影响。在高搅拌速度(100 r/min)对一级动力学方程拟合较好,Higuchi方程拟合相关性降低,西青果颗粒溶出机制只为Fick扩散。其原因是由于在低搅拌速度下颗粒的溶蚀过程影响药物溶出,在高搅拌速度下颗粒快速溶出,颗粒快速完成溶蚀过程。结果见表5。
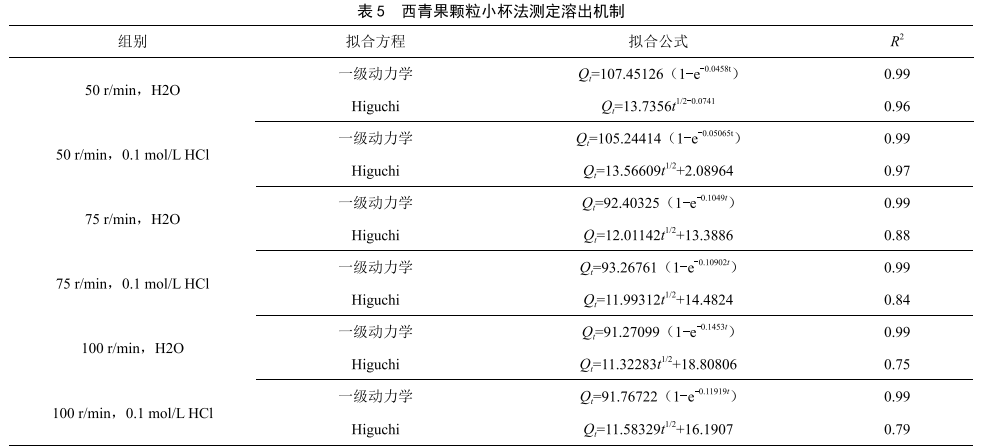
3 讨论
依托HPLC法,结合没食子酸在不同溶液之间溶出度的含量变化,有利于进一步分析中成药之间化学成分的溶出行为[6]。进行中药固体制剂的体外溶出研究是制剂质量控制与预测体内释药行为的有效手段,溶出条件的设置应模拟制剂在体内释药部位的生理环境。制剂在多种溶出环境中均能保持稳定可控的溶出特性是保证制剂在体内多种生理环境中良好溶出并保证生物利用度的前提[7]。不同的溶出测定方法会影响制剂的溶出曲线,小杯法在少量固体制剂的溶出测定中可提高溶出液的浓度以保证样品溶液满足检测限要求[8]。进行溶出曲线的溶出动力学分析可预测制剂在体内的溶出特性,并对溶出曲线进行精确控制。
参考文献
[1]林款,茹琴,梁征,等.西青果多酚的提取纯化及其抗氧化活性分析[J].食品研究与开发,2018,39(5):70-76.
[2]安硕,黄丽珍,李苏颖.正交设计优化西青果中没食子酸的提取工艺[J].河南医学高等专科学校学报,2017,29(5):500-502.
[3]王奉悦,李汝卓,汪敏等.西青果总鞣质中没食子酸和没食子酸乙酯含量测定及抗菌作用研究[J].吉林医药学院学报,2017,38(4):243-246.
[4]孙鹏.青果、西青果及诃子的鉴别与临床应用[J].临床医药文献杂志,2017,4(54):10673-10676.
[5]张嫱,黎翩,孙阳恩,等.中药固体制剂溶出行为研究进展[J].中国新药杂志,2019,28(20):2498-2501.
[6]孙国祥.中药整体质量标准体系构建和一致性评价步骤专题[J].中南药学,2019,17(3):321-331.
[7]王丽君,陈雅琴.法罗培南钠颗粒剂的制备及溶出方法学研究[J].辽宁化工,2014,43(3):246-247.
[8]郭怀宇,蒋家龙,陈金锋,等.中药固体制剂溶出度检测方法研究进展[J].广州化工,2017,45(11):24-32.
通信作者:巩腾飞(1989—),男,汉族,山东淄博人,硕士,主管药师。研究方向:药品检验。

相关热词搜索:
[责任编辑:]

 挪帝克开设京东旗舰店 与京东全球购达成战略合作
挪帝克开设京东旗舰店 与京东全球购达成战略合作
 2019《金博宝188官网注册 导刊》杂志订阅返百元红包!
2019《金博宝188官网注册 导刊》杂志订阅返百元红包!
 9月大事 | 市场监管总局开展2018年全国“质量月”活动
9月大事 | 市场监管总局开展2018年全国“质量月”活动
 盒装水果省事不卫生 实验解释3大疑问
盒装水果省事不卫生 实验解释3大疑问
 “食安中国网”手机站上线通知
“食安中国网”手机站上线通知
 食安中国网关于2015年春节放假的通知
食安中国网关于2015年春节放假的通知
 金博宝188官网注册 新动向讲座:权威解读金博宝188官网注册 中的过敏原问
金博宝188官网注册 新动向讲座:权威解读金博宝188官网注册 中的过敏原问 【采访ADM】力行不辍、多元发展,满足消费者的营养
【采访ADM】力行不辍、多元发展,满足消费者的营养 食品掺假与成分检测网络研讨会
食品掺假与成分检测网络研讨会 权威专家解读食品中的丙烯酰胺及含量控制措施,快来
权威专家解读食品中的丙烯酰胺及含量控制措施,快来 专家齐聚第三届全球金博宝188官网注册 共治论坛,启动金博宝188官网注册
专家齐聚第三届全球金博宝188官网注册 共治论坛,启动金博宝188官网注册





参与评论